Nilton Tabajara Herter
Daniel Sperb
Introdução
O tratamento dos tumores da glândula parótida apresenta um contexto de discussão assemelhado às controvérsias existentes no tratamento dos tumores da glândula tireóide. Parafraseando J. Crile que há um século em alto e bom som, afirmava que “o cirurgião ao proceder uma tireoidectomia, exercia a suprema arte da cirurgia” curando o paciente ao extirpar a doença e, preservando os nervos laríngeos e as glândulas paratireoides evitava as trágicas complicações de uma paralisia de cordas vocais e um grave hipoparatireoidismo.
Não menos graves são as complicações de uma parotidectomia executada por um cirurgião inexperiente, expondo o paciente aos riscos de uma ressecção incompleta de um tumor, bem como à grave sequela de uma paralisia facial. Assim, requer-se experiência, treinamento, conhecimento da patologia, da anatomia e todo o esmero possível na técnica cirúrgica.1
Na figura abaixo fica exemplificado um paciente pediátrico, com 9 anos de idade, no qual um cirurgião não especialista tentou ressecar uma neoplasia de parótida. A ressecção foi incompleta, causando contaminação tumoral de partes moles e disseminação linfática. O exame anátomo-patológico revelou tratar-se de carcinoma adenóide cístico.

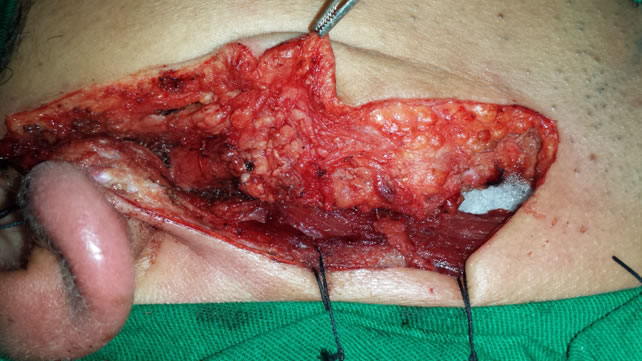
A cirurgia de resgate torna-se mais difícil, necessitando ressecção em bloco do tumor, pele, partes moles e parótida com esvaziamento cervical amplo, preservando-se as estruturas nobres não acometidas pela neoplasia. A foto seguinte demonstra a ressecção completa do tumor, parotidectomia total com preservação do nervo facial e seus ramos e esvaziamento cervical. A foto mostra ainda uma alteração anatômica interessante: a veia facial drenando apenas e diretamente para a jugular externa.

Todavia a decisão a ser tomada pelo cirurgião envolve algumas controvérsias de naturezas distintas:
Estes questionamentos serão abordados e discutidos baseados na experiência dos autores no Serviço de Cirurgia de Cabeça e Pescoço do Hospital Santa Rita da Santa Casa de Misericórdia de Porto Alegre e no Hospital Moinhos de Vento.
As tumefações observadas na região parotídia habitualmente são de diagnóstico fácil para o especialista, mas podem constituir-se em armadilhas para o médico menos experiente.
Podemos encontrar cistos sebáceos, cistos dermóides, cistos branquiais e lipomas sob a forma de tumefações localizadas na região parotídia. As linfonodopatias, sejam de origem inflamatória ou neoplásica, primárias ou metastáticas são comuns nesta região. Com o novo aumento de incidência de pacientes com sífilis, é recomendado pesquisar VDRL nos exames sorológicos pré operatórios, pois já observamos pacientes com nódulo parotídeo cuja ecografia e ressonância nuclear magnética sugeriam adenoma pleomórfico cujo “tumor” desapareceu após tratamento com benzetacil para sífilis diagnosticada no pré operatório.
Os tumores de origem sialogênica constituem a causa mais comum de nódulos na região parotídia, mas tumores não sialogênicos como adenolipomas, hemangiomas, neuroninomas e até tumores ósseos originados na mandíbula entram na lista de diagnóstico diferencial.
Por fim enfermidades próprias das glândulas salivares podem simular tumores, como síndrome de Sjögren, parotidites crônicas, sialoectasias ductais, cálculos de ductos salivares, doença de Madelung e muitas outras.
O exame clínico é fundamental e o mais importante de todos. Seguem-se em importância a ecografia, a imagem de ressonância magnética, a tomografia computadorizada, a sialografia contrastada e a cintilografia das glândulas salivares. A punção aspirativa com agulha fina seguida de exame citopatológico deve ser considerada nos casos de tumores sólidos, se impondo quando há suspeita de malignidade, todavia a indicação é relativa nas formações císticas.1
Os adenomas pleomórficos e os linfoadenomas papilares linfomatosos são os mais comuns entre os tumores benignos, podendo ser múltiplos e bilaterais.
Dos tumores malignos os mais comuns são o carcinoma mucoepidermóide, carcinoma adenóide cístico ( cilindroma ), o carcinoma de células acinares e o carcinoma ex-adenoma pleomórfico. Todavia carcinomas ou melanomas metastáticos não são raros.
Curiosamente, a distribuição dos tumores e seus tipos histológicos estão ligados ao tamanho da glândula salivar. A parótida, maior glândula salivar, é sede de 80% dos tumores das glândulas salivares, 10 a 20% dos tumores se originam nas glândulas submandibulares e o restante ocorre nas glândulas sublinguais ou nas salivares menores. Porém, dentre os tumores originados nas parótidas, 80% são benignos, nas submandibulares 40 a 60% são benignos, enquanto nas sublinguais e glândulas salivares menores o índice de benignidade é de apenas 18 a 30%.1
Como regra geral podemos dizer que:
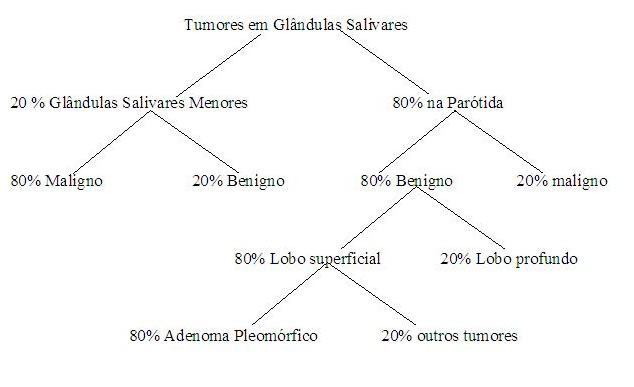
Conclui-se que submeter um paciente a uma intervenção cirúrgica sem um diagnóstico preciso constitui-se numa conduta arriscada e com possíveis consequências imprevisíveis.
A localização precisa do tumor é fundamental determinando se está no lobo superficial ou no lobo profundo da parótida. Outra questão de relevância é a multicentricidade do tumor, se os contornos estão bem definidos e se há ou houve algum compromisso da função do nervo facial. As dimensões do tumor são relevantes para a abordagem cirúrgica. Tratando-se de tumores malignos impõe-se a classificação pelo sistema TNM e o estadiamento clínico pela UICC.
A ultrassonografia com estudo Doppler colorido do nódulo realizada por radiologista experiente e a ressonância nuclear magnética se complementam na avaliação pré operatória. A qualidade da imagem da ressonância nuclear magnética das parótidas também facilita as explicações sobre a cirurgia ao paciente. Tomografia computadorizada se torna útil para avaliar comprometimento ósseo.
A extensão da cirurgia é uma das questões mais controversas em cirurgia para o tratamento dos tumores de glândulas parótidas. Nossa experiência indica que nos tumores malignos a cirurgia deverá ser radical, implicando sempre em parotidectomia total com preservação do nervo facial quando não houver invasão direta do mesmo pelo tumor. A radioterapia pós-operatória deve ser considerada. O esvaziamento cervical será do tipo eletivo.
Embora a maioria dos centros indique no mínimo parotidectomia superficial em todos os pacientes com tumores parotídeos2, achamos que muitos destes pacientes estão sendo submetidos a “over-treatment”. Nos tumores benignos adotamos uma atitude mais conservadora, realizando a dissecção extracapsular do tumor e preservando a parótida em tumores com até 3 cm de diâmetro.1
Para tanto a cirurgia deverá ser conduzida com a máxima delicadeza possível, utilizando-se dissecção romba extra-capsular eventualmente com o auxílio de micro torundas. Nunca pressionar contra o tumor e sempre lembrando que o adenoma pleomórfico é multi-lobulado. O nervo facial deve ser identificado, mas nem sempre sua dissecção é necessária. O acesso ao tumor é feito mediante uma incisão sobre o parênquima glandular em sentido transverso se o tumor estiver localizado nas porções frontais da glândula. Se o tumor estiver em região retromandibular utilizamos uma incisão vertical, até a identificação do tumor, cuja enucleação deverá ser completa, sem ruptura da cápsula. O resultado pode ser considerado excelente em mãos hábeis. A indicação maior da técnica é em adenomas pleomórficos ou linfoepitelioma papilar linfomatoso.
Realizamos esta técnica há mais de 30 anos, e não observamos recidivas tumorais. A evolução da monitorização neurofisiológica trans-operatória e surgimento de equipamentos automatizados, com retorno sonoro para o cirurgião, tornaram a dissecção extracapsular mais segura3. Atualmente vários centros passaram a realizar dissecção extracapsular, confirmando a segurança do procedimento se realizado por cirurgiões especialistas em cirurgia das glândulas parótidas.3,4,5
Quando se realiza a dissecção extracapsular, é fundamental a presença de patologista na sala de cirurgia, pois pode ser necessário conversão do procedimento em casos de discrepância com a suspeita diagnóstica inicial.6
Neoplasias benignas do lobo profundo podem ser operadas por técnica semelhante7. O nervo facial é localizado em seu tronco e dissecado, sendo o lobo superficial parcialmente levantado para expor o lobo profundo. O nódulo do lobo profundo é ressecado por dissecção extracapsular e então o lobo superficial pode ser reposicionado sobre o nervo facial. O cuidado na dissecção deve ser redobrado, pois ruptura capsular leva a recidiva no espaço parafaríngeo.
A fotografia seguinte mostra o lobo superficial parotídeo levantado fixo ao sistema músculo aponeurótico da face e pele. O nervo facial e seus ramos foram dissecados sobre o adenoma pleomórfico do lobo profundo. A porção anterior da parótida não é dissecada para não comprometer a drenagem salivar.
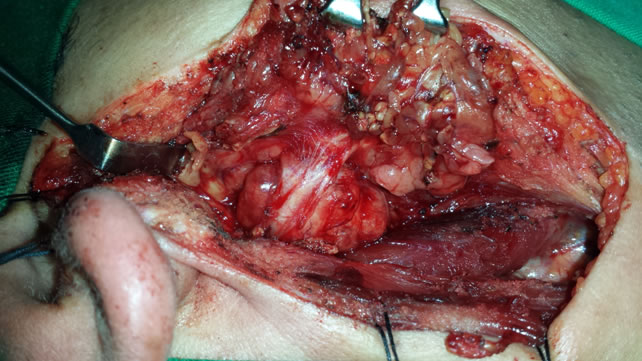
O nódulo do lobo profundo é ressecado por dissecção extracapsular. Podemos visualizar o nervo preservado e a cápsula tumoral intacta na peça cirúrgica, ressaltada com corante no exame anatomopatológico trans-operatório
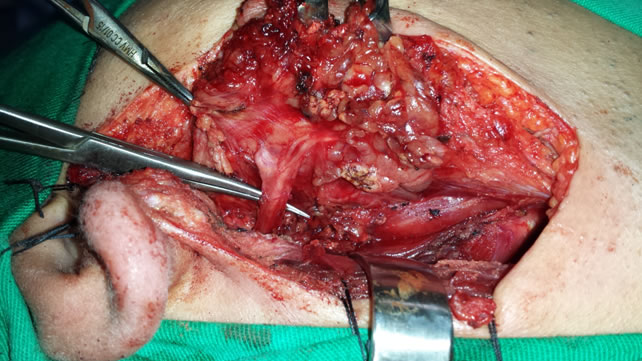
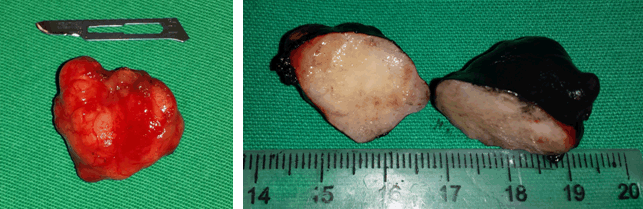
Por fim, observamos o lobo superficial reposicionado sobre o nervo facial. O paciente recebeu alta hospitalar no dia seguinte com perfeita função do nervo facial, sendo o dreno de penrose retirado 5 dias após a cirurgia. Não houve fístula salivar.
Utilizamos uma incisão com um componente vertical pré-auricular combinado com outra que contorna o lóbulo auricular e continua por mais alguns centímetros numa linha sobre o bordo anterior do músculo esternocleidomastoideo. A clássica incisão em “Y” pode criar uma cicatriz hipertrófica, especialmente no ponto de união das três suturas.
Nossa preferência e procurar o tronco do nervo facial logo abaixo de sua emergência um a dois centímetros do orifício estilomastóideo. Utilizamos uma divulção transversal com tesoura de dissecção romba, lembrando que o nervo pode estar deslocado em qualquer sentido pela pressão do tumor.
Consideramos fundamental para a identificação do nervo, o conhecimento de sua anatomia, topografia e sintopia. A iluminação do campo cirúrgico e uma perfeita hemostasia são muito importantes. A magnificação de imagens com o uso de lentes é benéfica e o uso do monitoramento do nervo não é essencial, exceto em recidivas ou para encontrar ramos periféricos.
O nervo grande auricular é o responsável pela inervação sensitiva do lóbulo auricular e sua secção implicará numa anestesia do lóbulo. A dissecção do nervo não é difícil e toma cerca de quinze minutos do tempo cirúrgico. O mesmo é encontrado ao elevar-se o retalho cutâneo posterior e, a partir daí poderá ser dissecado e preservado, principalmente nas cirurgias com dissecção extracapsular.
A fístula salivar poderá ser evitada com sutura cuidadosa do parênquima glandular usando fio absorvível. Quando usado dreno tipo porto-vac, este permanece uma média de três dias em vácuo, podendo ser seccionado e mantido mais alguns dias até que cesse a drenagem. O uso de hemostáticos absorvíveis e dreno tipo penrose permite alta hospitalar precoce e retirada ambulatorial do dreno. Eventual fístula salivar já estará orientada e encontra resolução expontânea em poucos dias.
A síndrome de Lucy Frey é uma complicação incômoda que decorre da regeneração de fibras nervosas do sistema nervoso autônomo da glândula parótida e que passam a inervar as glândulas sudoríparas cervicofaciais. Os sintomas podem variar de uma hiperemia regional durante a mastigação alimentar até uma intensa sudorese local, bastante desagradável. Esta ocorrência é rara nas dissecções extracapsulares todavia é frequente nas parotidectomias totais ou subtotais3. Para sua prevenção, poderemos preparar um retalho muscular do platisma e interpô-lo entre a pele e o leito da parotidectomia.
A radioterapia complementar deverá ser indicada em casos de tumores de alto grau de malignidade, casos de margens cirúrgicas insuficientes ou alguns casos de linfomas. Nos pacientes com doença avançada e histologia de alto grau o tratamento radioterápico complementar tem efeito positivo na sobrevida. Radioterapia exclusiva pode ser indicada em tratamentos paliativos 1.
A radioterapia pós-operatória em tumores malignos está indicada, mas vemos sua indicação muito restrita em tumores benignos, especialmente em jovens devido ao risco de transformação de uma neoplasia benigna em maligna, bem como o possível advento de uma neoplasia maligna radio-induzida.
O papel da quimioterapia associada a radioterapia ainda é incerto. Não há ainda evidência robusta que a quimioterapia melhore a resposta. Existe protocolo de estudo multicêntrico em andamento para tentar responder esta questão.8
Conclusões
Embora quase todos os aspectos que envolvam o diagnóstico e o tratamento dos tumores de parótidas sejam objeto de controvérsia, entendemos ser consenso as seguintes práticas:
Bibliografia:
1- Herter, NT; Sperb, D – Neoplasias de Glândulas Salivares – In: Tratado de Clínica Médica – Lopes, AC. Segunda edição pag 3127 a 3129
2-Kadletz, L; Grasl, S; Grasl, MC et all. Extracapsular dissection versus superficial parotidectomy in benign parotid gland tumors: The Vienna Medical School experience . Published online 5 October 2016 in Wiley Online Library (wileyonlinelibrary.com). DOI 10.1002/hed.24598
3-Riffat, F; Mahrous, AK; Buchanan, Maet all. Safety of Extracapsular Dissection in Benign Superficial Parotid Lesions. J. Maxillofac. Oral Surg. (Oct-Dec 2012) 11(4):407–410
4-Gupte, S; Sorathia, R; Shetye, A et All. Extracapsular dissection of pleomorphic adenoma in the parotid gland: A case report and review of the literature. Contemp Clin Dent 2014 Jan-Mar; 5(1): 99–101.
5-Smith, SL; Komisar, A Limited Parotidectomy: The Role of Extracapsular Dissection in Parotid Gland Neoplasms. Laryngoscope 117(7):1163-1167, July 2007.
6-Ogawa, AI; Takemoto, LE; Navarro,Pl Neoplasias de Glândulas Salivares Arq. Int. Otorrinolaringol. / Intl. Arch. Otorhinolaryngol.,São Paulo, v.12, n.3, p. 409-418, 2008
7-Hussain, A; Murray DP; Preservation of the superficial lobe for deep-lobe parotid tumors: a better aesthetic outcome. Ear Nose Throut J. 2005 Aug;84(8):518, 520-2, 524.
8-Rodriguez, C; Adelstein DJ. RTOG 1008A Randomized Phase II/Phase III Study of Adjuvant Concurrent Radiation and Chemotherapy versus Radiation Alone in Resected High-Risk Malignant Salivary Gland Tumors https://www.rtog.org/ClinicalTrials/ProtocolTable/StudyDetails.aspx?study=1008